Astrocitomul
Autor: Dolfi Alexandra , publicat la 02-07-2014
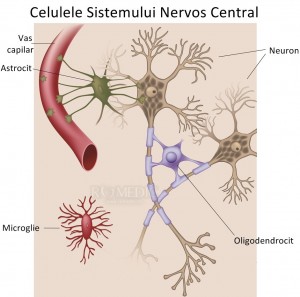
Astrocitoamele sunt neoplasme ale sistemului nervos central derivate din astrocite, care sunt celule gliale.
ExistƒÉ douƒÉ clase de tumori astrocitare »ôi anume: unele cu zone înguste de infiltra»õie (astrocitom pilocitic, astrocitom subependimar cu celule gigante, xantoastrocitom pleomorfic) »ôi unele cu zone difuze de infiltra»õie (astrocitom low-grade, astrocitom anaplastic, glioblastom). Membrii celui de-al doilea grup au în comun numeroase caracteristici inclusiv capacitatea de a se dezvolta la orice nivel al sistemului nervos central, cu o preferin»õƒÉ pentru emisferele cerebrale; apar mai frecvent la adul»õi; au proprietƒÉ»õi histopatologice heterogene »ôi un comportament biologic heterogen; infiltreazƒÉ difuz sau contiguu structurile sistemului nervos central indiferent de stadiul lor histologic »ôi au capacitatea de a progresa cƒÉtre stadii foarte avansate.
Există numeroase scheme de stadializare tumorală bazate pe caracteristicile fiziopatologice ale astrocitoamelor printre care și sistemul de grading Bailey si Cushing, gradele I-IV Kernohan, gradele I-IV World Health Organization și gradele 1-4 St. Anne/ Mayo. Gradul histologic al tumorii este determinat de analiza regiunilor tumorale cu cel mai mare grad de anaplazie (care conțin cel mai mare număr de celule nediferențiate). Gradul de anaplazie al tumorii este un factor predictiv negativ pentru progresia acestuia.
Schema de grading tumoral cel mai frecvent utilizată este cea a World Health Organization (WHO) care se bazează pe gradul de atipie nucleară a celulelor tumorale, activitatea mitotică, celularitate, proliferare vasculară și necroză. WHO gradul I corespunde astrocitomului pilocitar, WHO gradul II corespunde astrocitomului difuz low- grade, WHO gradul III corespunde astrocitomului anaplastic, iar WHO gradul IV corespunde glioblastomului multiform.
Astrocitoamele infiltrative difuze low-grade progreseazƒÉ foarte lent comparativ cu formele avansate, maligne. Timpul de dublare al unui astrocitom infiltrativ low-grade este de 4 ori mai mic decât cel al unui astrocitom anaplastic. În cazul astrocitomului low-grade trec câ»õiva ani de la simtomele ini»õiale »ôi stabilirea diagnosticului deoarece primele simptome trec aproape neobservate »ôi pacientul nu se prezintƒÉ la medic. Intervalul mediu calculat pentru aceste cazuri este de 3, 5 ani. Evolu»õia clinicƒÉ este marcatƒÉ de deteriorare gradatƒÉ a stƒÉrii generale a pacientului, numai în 15% din cazuri apƒÉrând o deteriorare bruscƒÉ a stƒÉrii generale. Convulsiile, în general generalizate sunt simptomul ini»õial la mai mult de jumƒÉtate din pacien»õii cu astrocitom low-grade.
Pacien»õii cu astrocitom anaplastic evolueazƒÉ mai rapid, rata de cre»ôtere a tumorii »ôi intervalul dintre apari»õia simptomului »ôi punerea diagnosticului situându-se între astrocitoamele low-grade »ôi glioblastoame. Intervalul mediu dintre apari»õia simptomelor »ôi diagnostic este 1, 5-2 ani. Comparativ cu astrocitoamele low-grade, convulsiile sunt mult mai pu»õin întâlnite, cele mai frecvente simptome fiind durerile de cap, status mental alterat »ôi deficite neurologice focale.
Raportul frecvenței astrocitoamelor la populația masculină versus populația feminină este 1,87:1 pentru astrocitoamele anaplastice.
Cele mai multe cazuri de astrocitom pilocitar sunt diagnosticate în primele douƒÉ decade de via»õƒÉ. Spre deosebire de aceasta, cel mai înalt grad de inciden»õƒÉ pentru astrocitoamele low –grade îl reprezintƒÉ vârsta de 30-40 de ani, la fel »ôi pentru astrocitomul anaplastic.
O atenție ridicată trebuie acordată semnelor de hipertensiune intracraniană precum cefaleea, greața și vărsăturile incoercibile, alterarea stării de alertă, alterarea cogniției, edemul papilar și ataxia. Acestea sunt sugestive pentru efectul de masă determinat de către tumoră, fiind asociate cu hidrocefalie și risc de herniere a encefalului prin gaura occipitală cu stop cardiorespirator. Lateralizarea semnelor neurologice precum paraliziile de nerv cranian, hemipareza, alterarea sensibilității, alterarea reflexelor osteotendinoase și prezența reflexelor neurologice patologice (semnele Hoffman și Babinski) trebuie analizate. Odată ce anomaliile neurologice sunt observate la examenul clinic, este obligatorie efectuarea testelor imagistice.
Etiologia astrocitoamelor difuze low-grade a fost asociatƒÉ cu numeroase boli »ôi expunere la factori de risc. S-au identificat însƒÉ prin studii clinice numai doi factori de risc »ôi anume iradierea terapeuticƒÉ pentru tratamentul cancerului »ôi expunerea la nitrozuree. De»ôi utilizarea extensivƒÉ a telefoanelor mobile este consideratƒÉ a fi un factor de risc pentru dezvoltarea tumorilor cerebrale, nu existƒÉ studii concludente în acest sens.
Copiii care au primit iradiere profilacticƒÉ pentru leucemia limfoblasticƒÉ acutƒÉ au un risc de 22 de ori mai mare de a dezvolta neoplasme de sistem nervos central, mai precis astrocitoame de gradul II, III sau IV în urmƒÉtorii 5-10 ani. Iradierea adenoamelor de glandƒÉ hipofizarƒÉ reprezintƒÉ de asemenea un factor de risc, ace»ôti pacien»õi având un risc de 16 ori mai mare pentru apari»õia glioamelor.
Astrocitoame cu determinism genetic s-au descoperit în familiile cu membri suferinzi de sindrom Turcot, neurofibromatozƒÉ 1 »ôi sindrom Li Fraumeni (muta»õii ale genei supresoare tumorale p53).
Dezvoltarea și progresia astrocitoamelor a fost asociată și cu mutația unor căi moleculare de comunicare intercelulară precum calea p53-MDM-p21 și p16-p15-CDK4-CDK6-RB. Două treimi din astrocitoamele difuze low-grade prezintă mutații ale genei supresoare tumorale p53.
Răspunsul la diferiți agenți citostatici a fost studiat comparativ cu structura genetică a celulelor tumorale. Prin urmare s-a descoperit că pacienții cu oligodendroglioame care prezintă modificări la nivelul unei anumite benzi a cromozomului 1 au răspuns mai bun la procarbazină și vincristină.
Nu existƒÉ teste de laborator specifice pentru diagnosticul astrocitoamelor. Se realizeazƒÉ testele de rutinƒÉ precum hemoleucogramƒÉ, uree, creatininƒÉ, glicemie, transaminaze, glucozƒÉ, ionogramƒÉ, timp de protrombinƒÉ »ôi timp de tromboplastinƒÉ par»õial activatƒÉ. Acestea nu sunt foarte utile pentru diagnostic însƒÉ sunt utile în supravegherea metabolicƒÉ a pacientului.
Computer Tomografia »ôi Rezonan»õa MagneticƒÉ NuclearƒÉ sunt cele mai utilizate teste imagistice în diagnosticul »ôi stadializarea tumoralƒÉ a astrocitoamelor. Rezonan»õa MagneticƒÉ este consideratƒÉ investiga»õia standard dar »ôi CT oferƒÉ imagini foarte bune.
Pe o scanare CT astrocitoamele low-grade apar ca mase hipodense, omogene, care nu se încarcƒÉ cu contrast. ÎnsƒÉ în cursul evolu»õiei tumorii pot sƒÉ aparƒÉ u»ôoarƒÉ încƒÉrcare cu contrast, calcificƒÉri »ôi structuri chistice la nivel tumoral. În cazul în care se descoperƒÉ o masƒÉ tumoralƒÉ adiacentƒÉ care se încarcƒÉ foarte mult cu contrast, »ôi multiple leziuni adiacente, trebuie suspectatƒÉ prezen»õa metastazelor. Se va realiza apoi scanarea sistematizatƒÉ a întregului corp cuprinzând torace, abdomen »ôi pelvis pentru a se eviden»õia metastazele diseminate la nivelul altor organe.
Astrocitoamele anaplastice apar de asemenea ca mase slab definite, omogene »ôi hipodense. Pot apƒÉrea însƒÉ »ôi ca leziuni cu areale alternante de hipodensitate »ôi hiperdensitate. Spre deosebire de astrocitoamele low grade, acestea se încarcƒÉ par»õial cu contrast.
Pe RMN, astrocitoamele sunt în general izointense în T1 »ôi hiperintense în T2. În timp ce astrocitoamele low-grade se încarcƒÉ foarte rar cu contrast, astrocitoamele anaplastice se încarcƒÉ în general cu substan»õƒÉ de contrast paramagneticƒÉ.
Angiografia poate fi utilizatƒÉ pentru eviden»õierea malforma»õiilor vasculare »ôi pentru evaluarea neovasculariza»õiei tumorale. În cazul astrocitoamelor low-grade, masa tumoralƒÉ este avascularƒÉ, însƒÉ în leziunile high-grade putem observa vasculariza»õie tumoralƒÉ.
Actualmente se folosesc teste imagistice intraoperator pentru controlul interven»õiei »ôi gidare. Acestea constituie în principal în rezonan»õƒÉ magneticƒÉ de mare rezolu»õie.
Crizele epileptice sunt foarte frecvent asociate cu astrocitoame prin urmare Electroencefalograma este frecvent utilizată pentru a evalua și monitoriza activitatea focarelor epileptice.
Scanările cu radionuclizi precum PET (tomografia cu emisie de pozitroni) și scintigrafia cu technețiu studiază metabolismul tumoral și funcția cerebrală. PET și SPECT se pot utiliza pentru diferențierea unei tumori solide de edem, pentru diferențierea unei recurențe tumorale de necroza de iradiere și pentru localizarea diferitelor structuri ale sistemului nervos central.
Activitatea metabolicƒÉ determinatƒÉ cu ajutorul scintigrafiei cu radionuclizi poate fi utilizatƒÉ pentru determinarea gradului de activitate al tumorii. Leziunile hipermetabolice corespund în general unor tumori cu grad mare de anaplazie »ôi agresive.
Pentru evaluarea riscului preoperator se efectuează obligatoriu Electrocardiogramă și radiografie cardio-pulmonară față și profil.
Punc»õia lombarƒÉ la pacien»õii cu astrocitoame cerebrale trebuie efectuatƒÉ cu maximum de precau»õie datoritƒÉ riscului de herniere cerebralƒÉ datorat presiunii crescute a lichidului cefalorahidian. Studiul lichidului cefalorahidian nu intrƒÉ în protocolul pentru diagnosticul astrocitoamelor însƒÉ poate fi utilizat pentru eliminarea altor entitƒÉ»õi de diagnostic diferen»õial precum metastaze cerebrale ale unor tumori viscerale, limfoame, meduloblastoame.
Există patru variante histologice ale astrocitomului difuz infiltrativ low grade: protoplasmic, gemistocitic, fibrilar și mixt.
Astrocitoamele protoplastice sunt în general situate la nivelul scoar»õei cerebrale »ôi au celule tumorale care con»õin predominant citoplasmƒÉ. Constituie aproximativ 28% din totalul astrocitoamelor infiltrative.
Astrocitomul gemistocitic este în general prezent la nivelul emisferelor cerebrale la adult »ôi con»õine celule mari, rotunde cu citoplasmƒÉ eozinofilicƒÉ »ôi excentricƒÉ. Constituie 5-10% din total.
Astrocitoamele fibrilare sunt cea mai frecventă variantă histologică de astrocitom low-grade și seamănă cu celulele materiei albe cerebrale fiind compuse din celule mici, ovale și bine diferențiate. Tumorile, spre deosebire de substanța albă cerebrală au o celularitate mai crescută și o rețea fibrilară mai bine dezvoltată. Pentru identificarea astrocitoamelor fibrilare se utilizează markeri pentru proteina glială acidă fibrilară (GFAP).
Astrocitoamele anaplastice, comparativ cu astrocitoamele low-grade au o tendință de a se extinde regional și conțin celule cu un grad mare de anaplazie, un nucleu complex, mitoze crescute, variabilitate citoplasmatică mare și proliferare crescută a celulelor endoteliale.
Stadializarea histologicƒÉ a tumorii este imortantƒÉ atunci când se dore»ôte determinarea prognosticului pacientului. Spre deosebire de alte tumori sistemice, metastazele extracraniene ale astrocitoamelor sunt foarte rare. Declinul clinic al pacientului »ôi morbiditatea »ôi mortalitatea asociate tumorii sunt în general datorate efectelor locale de masƒÉ care determinƒÉ hipertensiune intracranianƒÉ sau recidivei tumorale.
În general, pacien»õii cu tumori cerebrale sunt îngriji»õi de cƒÉtre un neurolog în colaborare cu un specialist în neurooncologie.
Neurologul este cel care consultă primul pacientul, face examenul clinic neurologic elaborat și corelează simtomatologia cu descoperirile imagistice și histopatologice. Tot neurologul prescrie și tratamentul antiepileptic.
Neurochirurgul stabilește riscurile și beneficiile intervenției chirurgicale, realizează biopsia stereotactică și tratează hipertensiunea intracraniană prin efectuarea de șunturi și deviații ventriculare.
Neurooncologul este acela care vine cu un plan terapeutic în urma evaluƒÉrii histologice. Va prescrie chimioterapia »ôi/ sau radioterapia adjuvantƒÉ.
Nu există un standard de tratament acceptat pentru astrocitoamele low-grade sau anaplastice. Un studiu recent arată că radioterapia adjuvantă pentru astrocitoamele pilocitare crește rata de supraviețuire de la 5 la 10 ani comparativ cu pacienții netratați.
Decizia în ce prive»ôte interven»õia operatorie »ôi utilizarea agen»õilor citostatici »ôi/sau a radioterapie trebuie luatƒÉ în grup, într-o echipƒÉ medicalƒÉ în care sƒÉ se afle un neurochirurg, un neurolog »ôi un oncolog.
Astrocitoamele anaplastice sunt tratate în general cu chirurgie, radioterapie »ôi chimioterapie adjuvantƒÉ. Sunt mult mai repede responsive la chimioterapie comparativ cu glioblastoamele. Astrocitoamele anaplastice recurente se trateazƒÉ cu nitrozuree »ôi temozolomid (agen»õi citostatici).
Tratamentul astrocitoamelor infiltrative low-grade este mult mai controversat. Rolurile rezec»õiei chirurgicale maximale, al radioterapiei »ôi al agen»õilor chimioterapici nu sunt încƒÉ foarte clare datoritƒÉ faptului cƒÉ aceste tumori debuteazƒÉ în general la vârste tinere, evolueazƒÉ inconstant, iar interven»õia chirurgicalƒÉ este asociatƒÉ cu un grad mare de morbiditate »ôi mortalitate.
Pacienții cu astrocitom și istoric de convulsii vor primi terapie anticonvulsivantă cu monitorizarea concentrației sanguine a medicamentului. Utilizarea profilactică a anticonvulsivantelor la pacienții cu astrocitom fără antecedente de convulsii nu s-a dovedit eficace.
Utilizarea corticosteroizilor precum dexametazona determinƒÉ o înbunƒÉtƒÉ»õire rapidƒÉ a stƒÉrii pacientului care a suferit o hipertensiune intracranianƒÉ ca urmare a efectului de masƒÉ determinat de tumorƒÉ, deoarece reduce edemul peritumoral. În acela»ôi timp cu administrarea corticosteroizilor trebuie obligatoriu fƒÉcutƒÉ profilaxia ulcerului gastroduodenal cu inhibitori de pompƒÉ de protoni precum omeprazolul.
Glioamele de trunchi cerebral reprezintƒÉ o clasƒÉ aparte în tratamentul astrocitoamelor întrucât apar în general în popula»õia pediatricƒÉ, în general la vîrste cuprinse între 7 »ôi 9 ani. Tratamentul »ôi prognosticul acestor tumori depinde de gradul de extindere localƒÉ a tumorii.
Glioamele difuze de trunchi cerebral reprezintƒÉ majoritatea tumorilor de trunchi cerebral, în general localizate la nivelul pun»õii, necircumscrise pe RMN. Sunt în genral astrocitoame fibrilare maligne WHO gradul III sau IV care infiltreazƒÉ materia albƒÉ »ôi tracturile din trunchiul cerebral »ôi talamus »ôi au un prognostic nefast, fiind în general fatale. Prezentarea clinicƒÉ a acestor tumori include simptome precum ataxia, semne cerebeloase »ôi semne piramidale. Nu s-au eviden»õiat avantaje ale interven»õiei chirurgicale în principal datoritƒÉ localizƒÉrii acestor tumori »ôi datoritƒÉ naturii lor agresive. Corticosteroizii au un efect limitat prin reducerea edemului în timp ce radioterapia determinƒÉ pentru un scurt timp ameliorarea stƒÉrii generale, întrucât chiar cu radioterapie în doze mari, supravie»õuirea nu depƒÉ»ôe»ôte 1 an.
Glioamele focale de trunchi cerebral sunt în general încadrate în clasele WHO I sau II, bine circumscrise pe RMN, se încarcƒÉ variabil cu contrast »ôi sunt mult mai frecvent în bulb. Au un prognostic mai bun decât glioamele difuze de trunchi cerebral, chirurgia fiind tratamentul de elec»õie în acest caz. Hidrocefalia obstructivƒÉ este foarte frecventƒÉ, fiind tratatƒÉ tot chirurgical, fie endoscopic, fie prin ventriculostomie a ventriculului III fie prin plasarea de »ôunt ventriculo peritoneal.
Rolurile principale ale chirurgiei în cazul unui pacient cu astrocitom sunt sƒÉ îndepƒÉrteze cât mai mutl din tumorƒÉ »ôi sƒÉ ofere »õesut pentru diagnosticul histologic permi»õând astfel realizarea unui plan viitor de tratament cu terapie adjuvantƒÉ »ôi stabilirea prognosticului pacientului.
Biopsia stereotacticƒÉ este o procedurƒÉ simplƒÉ »ôi sigurƒÉ pentru punerea diagnosticului de»õesut. Riscul este însƒÉ de hemoragie intracranianƒÉ. Pentru scƒÉderea presiunii intracraniene la pacien»õii cu hipertensiune determinatƒÉ de efectul de masƒÉ tumoralƒÉ »ôi de edem se poate monta un »ôunt ventriculoperitoneal sau un drenaj ventricular extern. AceastƒÉ procedurƒÉ trebuie realizatƒÉ înaintea efectuƒÉrii interven»õiei chirurgicale.
Rezec»õia totalƒÉ a astrocitomului este frecvent imposibilƒÉ deoarece aceste tumori invadeazƒÉ frecvent regiuni inaccesibile ale creierului »ôi infiltreazƒÉ scoar»õa cerebralƒÉ la nivele detectate doar microscopic. ÎnsƒÉ, rezec»õia chirurgicalƒÉ pune diagnosticul histologic al tumorii »ôi cre»ôte calitatea vie»õii pacientului precum »ôi durata de via»õƒÉ.
Managementul astrocitoamelor low-grade este controversat. Tumora poate fi stabilƒÉ radiologic »ôi latentƒÉ din punct de vedere clinic pentru perioade lungi de timp de la prezentarea ini»õialƒÉ la medic. Ca op»õiuni terapeutice existƒÉ observa»õia, iradierea »ôi rezec»õia cu sau fƒÉrƒÉ iradiere. DacƒÉ astrocitomul nu a fost excizat chirurgical complet, trebuie luatƒÉ în considerare iradierea postoperatorie adjuvantƒÉ.
Neurologul va urmƒÉri pacientul pe termen lung pentru a observa progresia sau regresia semnelor neurologice »ôi pentru a manageria tratamentul cu corticosteroizi »ôi anticonvulsivante. Chimioterapia postoperatorie »ôi postiradiere cu nitrozuree are un beneficiu dovedit în cazul pacien»õilor cu astrocitoame maligne.
Frecven»õa cu care se vor efectua RMN-urile postoperatorii depinde de decizia neurochirurgului »ôi oncologului.
Este favorabil pentru astrocitoamele low-grade postoperator »ôi dupƒÉ terapia cu radia»õii. Timpul de supravie»õuire postoperator este în jur de 6-8 ani.
În cazul astrocitomului anaplastic, rata de supravie»õuire postoperator este de asemenea mare, 60-80% dintre pacien»õi supravie»õuind la 5 ani de la diagnostic. Factorii precum vîrsta tânƒÉrƒÉ, statusul nutri»õional »ôi metabolic adecvat »ôi extinderea mare a rezec»õiei asociatƒÉ cu iradiere în doze corespunzƒÉtoare pot cre»ôte mult durata de supravie»õuire.
ExistƒÉ douƒÉ clase de tumori astrocitare »ôi anume: unele cu zone înguste de infiltra»õie (astrocitom pilocitic, astrocitom subependimar cu celule gigante, xantoastrocitom pleomorfic) »ôi unele cu zone difuze de infiltra»õie (astrocitom low-grade, astrocitom anaplastic, glioblastom). Membrii celui de-al doilea grup au în comun numeroase caracteristici inclusiv capacitatea de a se dezvolta la orice nivel al sistemului nervos central, cu o preferin»õƒÉ pentru emisferele cerebrale; apar mai frecvent la adul»õi; au proprietƒÉ»õi histopatologice heterogene »ôi un comportament biologic heterogen; infiltreazƒÉ difuz sau contiguu structurile sistemului nervos central indiferent de stadiul lor histologic »ôi au capacitatea de a progresa cƒÉtre stadii foarte avansate.
Există numeroase scheme de stadializare tumorală bazate pe caracteristicile fiziopatologice ale astrocitoamelor printre care și sistemul de grading Bailey si Cushing, gradele I-IV Kernohan, gradele I-IV World Health Organization și gradele 1-4 St. Anne/ Mayo. Gradul histologic al tumorii este determinat de analiza regiunilor tumorale cu cel mai mare grad de anaplazie (care conțin cel mai mare număr de celule nediferențiate). Gradul de anaplazie al tumorii este un factor predictiv negativ pentru progresia acestuia.
Schema de grading tumoral cel mai frecvent utilizată este cea a World Health Organization (WHO) care se bazează pe gradul de atipie nucleară a celulelor tumorale, activitatea mitotică, celularitate, proliferare vasculară și necroză. WHO gradul I corespunde astrocitomului pilocitar, WHO gradul II corespunde astrocitomului difuz low- grade, WHO gradul III corespunde astrocitomului anaplastic, iar WHO gradul IV corespunde glioblastomului multiform.
Fiziopatologie
Efectele regionale asupra materialului nervos determinate de astrocitoame cuprind invazia, compresia »ôi distrugerea parenchimului cerebral. Hipoxia arterialƒÉ »ôi venoasƒÉ, competi»õia pentru nutrien»õi, eliberarea de produ»ôi metabolici toxici (radicali liberi, electroli»õi altera»õi, neurotransmi»õƒÉtori) »ôi eliberarea de factori de mediere celularƒÉ (citokine) interferƒÉ cu func»õionarea normalƒÉ a parenchimului cerebral. Presiunea intracranianƒÉ ridicatƒÉ atribuitƒÉ efectului direct de masƒÉ al tumorii, cre»ôterea volumului sanguin »ôi cre»ôterea volumului de lichid cefalorahidian pot determina sechele clinice secundare. Semnele neurologice »ôi simptomele atribuite astrocitoamelor derivƒÉ din perturbarea func»õiei sistemului nervos central. Semnele neurologice de focar (slƒÉbiciune muscularƒÉ, paralizie, deficite senzoriale, paralizii de nervi cranieni) »ôi convulsiile cu caracteristici variabile pot permite localizarea anatomicƒÉ a leziunii de cƒÉtre clinician.Astrocitoamele infiltrative difuze low-grade progreseazƒÉ foarte lent comparativ cu formele avansate, maligne. Timpul de dublare al unui astrocitom infiltrativ low-grade este de 4 ori mai mic decât cel al unui astrocitom anaplastic. În cazul astrocitomului low-grade trec câ»õiva ani de la simtomele ini»õiale »ôi stabilirea diagnosticului deoarece primele simptome trec aproape neobservate »ôi pacientul nu se prezintƒÉ la medic. Intervalul mediu calculat pentru aceste cazuri este de 3, 5 ani. Evolu»õia clinicƒÉ este marcatƒÉ de deteriorare gradatƒÉ a stƒÉrii generale a pacientului, numai în 15% din cazuri apƒÉrând o deteriorare bruscƒÉ a stƒÉrii generale. Convulsiile, în general generalizate sunt simptomul ini»õial la mai mult de jumƒÉtate din pacien»õii cu astrocitom low-grade.
Pacien»õii cu astrocitom anaplastic evolueazƒÉ mai rapid, rata de cre»ôtere a tumorii »ôi intervalul dintre apari»õia simptomului »ôi punerea diagnosticului situându-se între astrocitoamele low-grade »ôi glioblastoame. Intervalul mediu dintre apari»õia simptomelor »ôi diagnostic este 1, 5-2 ani. Comparativ cu astrocitoamele low-grade, convulsiile sunt mult mai pu»õin întâlnite, cele mai frecvente simptome fiind durerile de cap, status mental alterat »ôi deficite neurologice focale.
Epidemiologie
În Statele Unite ale Americii, inciden»õa anualƒÉ a astrocitomului este 5,4 cazuri la 100.000 de locuitori. Mortalitatea »ôi morbiditatea sunt strict corelate cu gradul histopatologic al astrocitomului. Ratele de supravie»õuire sunt aproximativ 10 ani de la diagnostic pentru astrocitoamele pilocitare (WHO grad I), 5 ani de la diagnostic pentru astrocitoamele difuze low grade (WHO grad II), 2-5 ani de la diagnostic pentru astrocitoamele anaplastice (WHO grad III) »ôi mai pu»õin de 1 an pentru glioblastoame (WHO grad IV).Raportul frecven»õei astrocitoamelor la popula»õia masculinƒÉ versus popula»õia femininƒÉ este 1,87:1 pentru astrocitoamele anaplastice.
Cele mai multe cazuri de astrocitom pilocitar sunt diagnosticate în primele douƒÉ decade de via»õƒÉ. Spre deosebire de aceasta, cel mai înalt grad de inciden»õƒÉ pentru astrocitoamele low –grade îl reprezintƒÉ vârsta de 30-40 de ani, la fel »ôi pentru astrocitomul anaplastic.
Istoricul bolii
Tipul de simptome neurologice dezvoltate de cƒÉtre un pacient cu astrocitom depinde de sediul anatomic unde se dezvoltƒÉ tumora, la nivelul sistemului nervos central. Alterarea statusului mental, dificultƒÉ»õile cognitive, cefaleea, anomaliile de câmp vizual, incapacitatea motorie, convulsiile, anomaliile senzoriale sau ataxia raportate de cƒÉtre pacient sau prezente în istoricul sƒÉu medical trebuie sƒÉ alerteze clinicianul cu privire la prezen»õa unei boli neurologice, necesitând teste viitoare de diagnostic. Prin urmare, testele imagistice precum CT »ôi RMN cu sau fƒÉrƒÉ contrast sunt indicate. Astrocitoamele mƒÉduvei spinƒÉrii sau ale trunchiului cerebral sunt mai pu»õin frecvente »ôi debuteazƒÉ în general cu semne motorii/senzoriale de afectare a nervilor cranieni.Examen clinic
Este obligatorie efectuarea unui examen neurologic detaliat în vederea evaluƒÉrii oricƒÉrui pacient cu astrocitom. Deoarece aceste tumori pot sƒÉ afecteze orice nivel al sistemului nervos central, inclusiv mƒÉduva spinƒÉrii »ôi se pot rƒÉspândi cƒÉtre regiunile distale ale sistemului nervos central, un examen clinic riguros orientat cƒÉtre toate componentele sistemuliu nervos este necesar pentru a se determina loca»õia »ôi gradul de extindere al afectƒÉrii nervoase.O aten»õie ridicatƒÉ trebuie acordatƒÉ semnelor de hipertensiune intracranianƒÉ precum cefaleea, grea»õa »ôi vƒÉrsƒÉturile incoercibile, alterarea stƒÉrii de alertƒÉ, alterarea cogni»õiei, edemul papilar »ôi ataxia. Acestea sunt sugestive pentru efectul de masƒÉ determinat de cƒÉtre tumorƒÉ, fiind asociate cu hidrocefalie »ôi risc de herniere a encefalului prin gaura occipitalƒÉ cu stop cardiorespirator. Lateralizarea semnelor neurologice precum paraliziile de nerv cranian, hemipareza, alterarea sensibilitƒÉ»õii, alterarea reflexelor osteotendinoase »ôi prezen»õa reflexelor neurologice patologice (semnele Hoffman »ôi Babinski) trebuie analizate. OdatƒÉ ce anomaliile neurologice sunt observate la examenul clinic, este obligatorie efectuarea testelor imagistice.
Cauze
Etiologia astrocitoamelor difuze low-grade a fost asociatƒÉ cu numeroase boli »ôi expunere la factori de risc. S-au identificat însƒÉ prin studii clinice numai doi factori de risc »ôi anume iradierea terapeuticƒÉ pentru tratamentul cancerului »ôi expunerea la nitrozuree. De»ôi utilizarea extensivƒÉ a telefoanelor mobile este consideratƒÉ a fi un factor de risc pentru dezvoltarea tumorilor cerebrale, nu existƒÉ studii concludente în acest sens. Copiii care au primit iradiere profilacticƒÉ pentru leucemia limfoblasticƒÉ acutƒÉ au un risc de 22 de ori mai mare de a dezvolta neoplasme de sistem nervos central, mai precis astrocitoame de gradul II, III sau IV în urmƒÉtorii 5-10 ani. Iradierea adenoamelor de glandƒÉ hipofizarƒÉ reprezintƒÉ de asemenea un factor de risc, ace»ôti pacien»õi având un risc de 16 ori mai mare pentru apari»õia glioamelor.
Astrocitoame cu determinism genetic s-au descoperit în familiile cu membri suferinzi de sindrom Turcot, neurofibromatozƒÉ 1 »ôi sindrom Li Fraumeni (muta»õii ale genei supresoare tumorale p53).
Dezvoltarea și progresia astrocitoamelor a fost asociată și cu mutația unor căi moleculare de comunicare intercelulară precum calea p53-MDM-p21 și p16-p15-CDK4-CDK6-RB. Două treimi din astrocitoamele difuze low-grade prezintă mutații ale genei supresoare tumorale p53.
Răspunsul la diferiți agenți citostatici a fost studiat comparativ cu structura genetică a celulelor tumorale. Prin urmare s-a descoperit că pacienții cu oligodendroglioame care prezintă modificări la nivelul unei anumite benzi a cromozomului 1 au răspuns mai bun la procarbazină și vincristină.
Teste de laborator
Nu existƒÉ teste de laborator specifice pentru diagnosticul astrocitoamelor. Se realizeazƒÉ testele de rutinƒÉ precum hemoleucogramƒÉ, uree, creatininƒÉ, glicemie, transaminaze, glucozƒÉ, ionogramƒÉ, timp de protrombinƒÉ »ôi timp de tromboplastinƒÉ par»õial activatƒÉ. Acestea nu sunt foarte utile pentru diagnostic însƒÉ sunt utile în supravegherea metabolicƒÉ a pacientului.
Teste imagistice
Computer Tomografia »ôi Rezonan»õa MagneticƒÉ NuclearƒÉ sunt cele mai utilizate teste imagistice în diagnosticul »ôi stadializarea tumoralƒÉ a astrocitoamelor. Rezonan»õa MagneticƒÉ este consideratƒÉ investiga»õia standard dar »ôi CT oferƒÉ imagini foarte bune. Pe o scanare CT astrocitoamele low-grade apar ca mase hipodense, omogene, care nu se încarcƒÉ cu contrast. ÎnsƒÉ în cursul evolu»õiei tumorii pot sƒÉ aparƒÉ u»ôoarƒÉ încƒÉrcare cu contrast, calcificƒÉri »ôi structuri chistice la nivel tumoral. În cazul în care se descoperƒÉ o masƒÉ tumoralƒÉ adiacentƒÉ care se încarcƒÉ foarte mult cu contrast, »ôi multiple leziuni adiacente, trebuie suspectatƒÉ prezen»õa metastazelor. Se va realiza apoi scanarea sistematizatƒÉ a întregului corp cuprinzând torace, abdomen »ôi pelvis pentru a se eviden»õia metastazele diseminate la nivelul altor organe.
Astrocitoamele anaplastice apar de asemenea ca mase slab definite, omogene »ôi hipodense. Pot apƒÉrea însƒÉ »ôi ca leziuni cu areale alternante de hipodensitate »ôi hiperdensitate. Spre deosebire de astrocitoamele low grade, acestea se încarcƒÉ par»õial cu contrast.
Pe RMN, astrocitoamele sunt în general izointense în T1 »ôi hiperintense în T2. În timp ce astrocitoamele low-grade se încarcƒÉ foarte rar cu contrast, astrocitoamele anaplastice se încarcƒÉ în general cu substan»õƒÉ de contrast paramagneticƒÉ.
Angiografia poate fi utilizatƒÉ pentru eviden»õierea malforma»õiilor vasculare »ôi pentru evaluarea neovasculariza»õiei tumorale. În cazul astrocitoamelor low-grade, masa tumoralƒÉ este avascularƒÉ, însƒÉ în leziunile high-grade putem observa vasculariza»õie tumoralƒÉ.
Actualmente se folosesc teste imagistice intraoperator pentru controlul interven»õiei »ôi gidare. Acestea constituie în principal în rezonan»õƒÉ magneticƒÉ de mare rezolu»õie.
Alte teste
Crizele epileptice sunt foarte frecvent asociate cu astrocitoame prin urmare Electroencefalograma este frecvent utilizată pentru a evalua și monitoriza activitatea focarelor epileptice. Scanările cu radionuclizi precum PET (tomografia cu emisie de pozitroni) și scintigrafia cu technețiu studiază metabolismul tumoral și funcția cerebrală. PET și SPECT se pot utiliza pentru diferențierea unei tumori solide de edem, pentru diferențierea unei recurențe tumorale de necroza de iradiere și pentru localizarea diferitelor structuri ale sistemului nervos central.
Activitatea metabolicƒÉ determinatƒÉ cu ajutorul scintigrafiei cu radionuclizi poate fi utilizatƒÉ pentru determinarea gradului de activitate al tumorii. Leziunile hipermetabolice corespund în general unor tumori cu grad mare de anaplazie »ôi agresive.
Pentru evaluarea riscului preoperator se efectuează obligatoriu Electrocardiogramă și radiografie cardio-pulmonară față și profil.
Punc»õia lombarƒÉ la pacien»õii cu astrocitoame cerebrale trebuie efectuatƒÉ cu maximum de precau»õie datoritƒÉ riscului de herniere cerebralƒÉ datorat presiunii crescute a lichidului cefalorahidian. Studiul lichidului cefalorahidian nu intrƒÉ în protocolul pentru diagnosticul astrocitoamelor însƒÉ poate fi utilizat pentru eliminarea altor entitƒÉ»õi de diagnostic diferen»õial precum metastaze cerebrale ale unor tumori viscerale, limfoame, meduloblastoame.
Anatomopatologie
ExistƒÉ patru variante histologice ale astrocitomului difuz infiltrativ low grade: protoplasmic, gemistocitic, fibrilar »ôi mixt. Astrocitoamele protoplastice sunt în general situate la nivelul scoar»õei cerebrale »ôi au celule tumorale care con»õin predominant citoplasmƒÉ. Constituie aproximativ 28% din totalul astrocitoamelor infiltrative.
Astrocitomul gemistocitic este în general prezent la nivelul emisferelor cerebrale la adult »ôi con»õine celule mari, rotunde cu citoplasmƒÉ eozinofilicƒÉ »ôi excentricƒÉ. Constituie 5-10% din total.
Astrocitoamele fibrilare sunt cea mai frecventă variantă histologică de astrocitom low-grade și seamănă cu celulele materiei albe cerebrale fiind compuse din celule mici, ovale și bine diferențiate. Tumorile, spre deosebire de substanța albă cerebrală au o celularitate mai crescută și o rețea fibrilară mai bine dezvoltată. Pentru identificarea astrocitoamelor fibrilare se utilizează markeri pentru proteina glială acidă fibrilară (GFAP).
Astrocitoamele anaplastice, comparativ cu astrocitoamele low-grade au o tendință de a se extinde regional și conțin celule cu un grad mare de anaplazie, un nucleu complex, mitoze crescute, variabilitate citoplasmatică mare și proliferare crescută a celulelor endoteliale.
Stadializarea histologicƒÉ a tumorii este imortantƒÉ atunci când se dore»ôte determinarea prognosticului pacientului. Spre deosebire de alte tumori sistemice, metastazele extracraniene ale astrocitoamelor sunt foarte rare. Declinul clinic al pacientului »ôi morbiditatea »ôi mortalitatea asociate tumorii sunt în general datorate efectelor locale de masƒÉ care determinƒÉ hipertensiune intracranianƒÉ sau recidivei tumorale.
Tratament
În general, pacien»õii cu tumori cerebrale sunt îngriji»õi de cƒÉtre un neurolog în colaborare cu un specialist în neurooncologie. Neurologul este cel care consultƒÉ primul pacientul, face examenul clinic neurologic elaborat »ôi coreleazƒÉ simtomatologia cu descoperirile imagistice »ôi histopatologice. Tot neurologul prescrie »ôi tratamentul antiepileptic.
Neurochirurgul stabilește riscurile și beneficiile intervenției chirurgicale, realizează biopsia stereotactică și tratează hipertensiunea intracraniană prin efectuarea de șunturi și deviații ventriculare.
Neurooncologul este acela care vine cu un plan terapeutic în urma evaluƒÉrii histologice. Va prescrie chimioterapia »ôi/ sau radioterapia adjuvantƒÉ.
Nu există un standard de tratament acceptat pentru astrocitoamele low-grade sau anaplastice. Un studiu recent arată că radioterapia adjuvantă pentru astrocitoamele pilocitare crește rata de supraviețuire de la 5 la 10 ani comparativ cu pacienții netratați.
Decizia în ce prive»ôte interven»õia operatorie »ôi utilizarea agen»õilor citostatici »ôi/sau a radioterapie trebuie luatƒÉ în grup, într-o echipƒÉ medicalƒÉ în care sƒÉ se afle un neurochirurg, un neurolog »ôi un oncolog.
Astrocitoamele anaplastice sunt tratate în general cu chirurgie, radioterapie »ôi chimioterapie adjuvantƒÉ. Sunt mult mai repede responsive la chimioterapie comparativ cu glioblastoamele. Astrocitoamele anaplastice recurente se trateazƒÉ cu nitrozuree »ôi temozolomid (agen»õi citostatici).
Tratamentul astrocitoamelor infiltrative low-grade este mult mai controversat. Rolurile rezec»õiei chirurgicale maximale, al radioterapiei »ôi al agen»õilor chimioterapici nu sunt încƒÉ foarte clare datoritƒÉ faptului cƒÉ aceste tumori debuteazƒÉ în general la vârste tinere, evolueazƒÉ inconstant, iar interven»õia chirurgicalƒÉ este asociatƒÉ cu un grad mare de morbiditate »ôi mortalitate.
Pacienții cu astrocitom și istoric de convulsii vor primi terapie anticonvulsivantă cu monitorizarea concentrației sanguine a medicamentului. Utilizarea profilactică a anticonvulsivantelor la pacienții cu astrocitom fără antecedente de convulsii nu s-a dovedit eficace.
Utilizarea corticosteroizilor precum dexametazona determinƒÉ o înbunƒÉtƒÉ»õire rapidƒÉ a stƒÉrii pacientului care a suferit o hipertensiune intracranianƒÉ ca urmare a efectului de masƒÉ determinat de tumorƒÉ, deoarece reduce edemul peritumoral. În acela»ôi timp cu administrarea corticosteroizilor trebuie obligatoriu fƒÉcutƒÉ profilaxia ulcerului gastroduodenal cu inhibitori de pompƒÉ de protoni precum omeprazolul.
Glioamele de trunchi cerebral
Glioamele de trunchi cerebral reprezintƒÉ o clasƒÉ aparte în tratamentul astrocitoamelor întrucât apar în general în popula»õia pediatricƒÉ, în general la vîrste cuprinse între 7 »ôi 9 ani. Tratamentul »ôi prognosticul acestor tumori depinde de gradul de extindere localƒÉ a tumorii.Glioamele difuze de trunchi cerebral reprezintƒÉ majoritatea tumorilor de trunchi cerebral, în general localizate la nivelul pun»õii, necircumscrise pe RMN. Sunt în genral astrocitoame fibrilare maligne WHO gradul III sau IV care infiltreazƒÉ materia albƒÉ »ôi tracturile din trunchiul cerebral »ôi talamus »ôi au un prognostic nefast, fiind în general fatale. Prezentarea clinicƒÉ a acestor tumori include simptome precum ataxia, semne cerebeloase »ôi semne piramidale. Nu s-au eviden»õiat avantaje ale interven»õiei chirurgicale în principal datoritƒÉ localizƒÉrii acestor tumori »ôi datoritƒÉ naturii lor agresive. Corticosteroizii au un efect limitat prin reducerea edemului în timp ce radioterapia determinƒÉ pentru un scurt timp ameliorarea stƒÉrii generale, întrucât chiar cu radioterapie în doze mari, supravie»õuirea nu depƒÉ»ôe»ôte 1 an.
Glioamele focale de trunchi cerebral sunt în general încadrate în clasele WHO I sau II, bine circumscrise pe RMN, se încarcƒÉ variabil cu contrast »ôi sunt mult mai frecvent în bulb. Au un prognostic mai bun decât glioamele difuze de trunchi cerebral, chirurgia fiind tratamentul de elec»õie în acest caz. Hidrocefalia obstructivƒÉ este foarte frecventƒÉ, fiind tratatƒÉ tot chirurgical, fie endoscopic, fie prin ventriculostomie a ventriculului III fie prin plasarea de »ôunt ventriculo peritoneal.
Tratament chirurgical
Rolurile principale ale chirurgiei în cazul unui pacient cu astrocitom sunt sƒÉ îndepƒÉrteze cât mai mutl din tumorƒÉ »ôi sƒÉ ofere »õesut pentru diagnosticul histologic permi»õând astfel realizarea unui plan viitor de tratament cu terapie adjuvantƒÉ »ôi stabilirea prognosticului pacientului. Biopsia stereotacticƒÉ este o procedurƒÉ simplƒÉ »ôi sigurƒÉ pentru punerea diagnosticului de»õesut. Riscul este însƒÉ de hemoragie intracranianƒÉ. Pentru scƒÉderea presiunii intracraniene la pacien»õii cu hipertensiune determinatƒÉ de efectul de masƒÉ tumoralƒÉ »ôi de edem se poate monta un »ôunt ventriculoperitoneal sau un drenaj ventricular extern. AceastƒÉ procedurƒÉ trebuie realizatƒÉ înaintea efectuƒÉrii interven»õiei chirurgicale.
Rezec»õia totalƒÉ a astrocitomului este frecvent imposibilƒÉ deoarece aceste tumori invadeazƒÉ frecvent regiuni inaccesibile ale creierului »ôi infiltreazƒÉ scoar»õa cerebralƒÉ la nivele detectate doar microscopic. ÎnsƒÉ, rezec»õia chirurgicalƒÉ pune diagnosticul histologic al tumorii »ôi cre»ôte calitatea vie»õii pacientului precum »ôi durata de via»õƒÉ.
Urmărirea postoperatorie
Managementul astrocitoamelor low-grade este controversat. Tumora poate fi stabilƒÉ radiologic »ôi latentƒÉ din punct de vedere clinic pentru perioade lungi de timp de la prezentarea ini»õialƒÉ la medic. Ca op»õiuni terapeutice existƒÉ observa»õia, iradierea »ôi rezec»õia cu sau fƒÉrƒÉ iradiere. DacƒÉ astrocitomul nu a fost excizat chirurgical complet, trebuie luatƒÉ în considerare iradierea postoperatorie adjuvantƒÉ.Neurologul va urmƒÉri pacientul pe termen lung pentru a observa progresia sau regresia semnelor neurologice »ôi pentru a manageria tratamentul cu corticosteroizi »ôi anticonvulsivante. Chimioterapia postoperatorie »ôi postiradiere cu nitrozuree are un beneficiu dovedit în cazul pacien»õilor cu astrocitoame maligne.
Frecven»õa cu care se vor efectua RMN-urile postoperatorii depinde de decizia neurochirurgului »ôi oncologului.
Prognostic
Este favorabil pentru astrocitoamele low-grade postoperator »ôi dupƒÉ terapia cu radia»õii. Timpul de supravie»õuire postoperator este în jur de 6-8 ani.În cazul astrocitomului anaplastic, rata de supravie»õuire postoperator este de asemenea mare, 60-80% dintre pacien»õi supravie»õuind la 5 ani de la diagnostic. Factorii precum vîrsta tânƒÉrƒÉ, statusul nutri»õional »ôi metabolic adecvat »ôi extinderea mare a rezec»õiei asociatƒÉ cu iradiere în doze corespunzƒÉtoare pot cre»ôte mult durata de supravie»õuire.
Publicat la 02-07-2014 | Vizite: 2593 | bibliografie
